Az agyi bioelektromos potenciálok közvetlenül a feltárt agykéreg felszínéről is elvezethetők. Emberen ezt az eljárást csak műtétek közben alkalmazzák, állatokon azonban kísérleti célból gyakran használt elektrofiziológiai módszer.
Altatott állatokon végzett akut kísérletekben, más technikákkal kombinálva (pl. farmakológiai vizsgálatok, párhuzamos intracelluláris, mikroelektródás elvezetés vagy kísérletes epilepszia) vezetnek el ECoG-t.
A rágcsálók agyi potenciáljainak amplitúdó- és frekvencia viszonyai némileg különböznek az emberi EEG kapcsán ismertetett mintázatoktól. Patkányokban a hippocampus csak néhány milliméterrel az agyfelszín alatt helyezkedik el, ezért az ECoG-ben megjelenik a hippocampalis eredetű théta aktivitás is. Az állatok β és δ tevékenysége nem különbözik lényegesen az emberétől. Megfigyelhető az állat alvási szintjének megfelelő ECoG mintázat változás.
Altatás
Nembutalból 40 mg/kg-ot, vagy a keverékből 0,4 ml/100g-ot adunk i.p. Az altatás kezdetét és a felhasznált altató mennyiségét regisztráljuk a jegyzőkönyvben. Mivel a ketamin-xilazin keverék hatása rövid ideig tart, óránként pótlólagos dózisokat adunk (0.1 ml/100 g).
Műtét
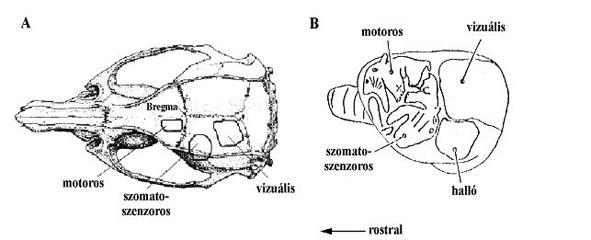
A műtét előtt meggyőződünk az altatás kellően mély voltáról (cornea reflex). Az állat fejét patkány-stereotaxiás készülékben rögzítjük (159. ábra). Ügyeljünk az állat kényelmes elhelyezkedésére, a nyomási pontokat és később a sebszéleket helyi érzéstelenítővel kezeljük (Lidokain, Procain). A koponyatetőn a bőrt a középvonal teljes hosszában nyitjuk, a koponyacsonton tapadó izmokat lefejtjük és a kötőszövetet eltávolítjuk. A koponyacsontokat papírvattával szárazra töröljük és a mellékelt ábra alapján ceruzával megjelöljük a vizsgálni kívánt kéregrésznek megfelelő területet (4. ábra).
4. ábra A: patkánykoponya felülnézetben, a csont felnyitásához megjelölt területekkel. B: patkány bal agyfélteke kéregszenzoros és mozgató területei szomatotópiás jelöléssel.
A mozgató kéreg bajusz képviseletének központja patkányban a bregmától laterális irányban, kb. 2.0 mm-re, rostralis irányban 2.0 mm-re található (ezen a ponton a kéreg direkt elektromos ingerlésével a bajusz szőrök mozgása váltható ki). A bajusz kérgi képviselete a szomatoszenzoros kérgen található, a bregmától laterális irányban, kb. 5.0 mm-re és caudalisan kb. 3.0 mm-re, míg az elsődleges látókéreg középső régiója a bregmától laterális irányban, kb. 3.0 mm-re laterálisan és caudalisan kb. 8.0 mm távolságban található. A kijelölt területen fogászati fúróval elvékonyítjuk a koponyacsontokat mindaddig, amíg a kéreg erei előtűnnek. Ekkor fiziológiás sóoldattal benedvesítjük a fúrás helyét, s finom sebészeti csipesszel betörjük azt, és kipattintjuk a koponyacsont korongot. Az állatot a műtét után legalább egy óráig pihenni hagyjuk. Az agyra a kiszáradás megelőzése érdekében langyos fiziológiás sóoldatot fecskendezünk, majd jól záró burával lefedjük. A kísérlet során mindvégig kísérjük figyelemmel az állatok testhőmérsékletét és az anesztézia megfelelő szintjét. Szükség esetén további altató adagolásáról gondoskodjunk.
A gömbvégű, ezüst elvezető elektródokat közvetlenül a feltárt agykéreg felszínére helyezzük. ECoG elvezetéséhez ajánlatos mindkét féltekén 2-2 elektródot elhelyezni, kiváltott potenciálok elvezetéséhez a megfelelő szenzoros área területére lerakunk egyet. Az indifferens elektródot célszerű rostralisan a koponyacsontra helyezni. Földelés céljából nagy felszínű ezüst drótot süllyesztünk a nyakbőr alá. Az agykérgi potenciálok elvezetése a humán EEG esetében ismertetett berendezéssel és technikával történhet.
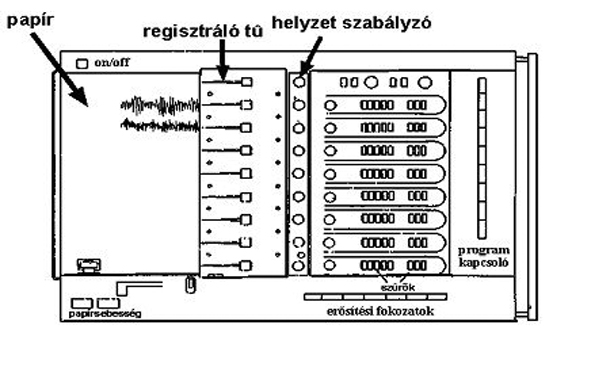
A jeleket biológiai erősítőn át Tektronix tároló oszcilloszkóp képernyőjén figyeljük és párhuzamosan 8 csatornás elektroencefalográffal íratjuk ki (5. ábra). A felvételnél 30 Hz -es felül- és 0.1 Hz -es alulvágó szűrőket alkalmazunk.
A kísérlet menete:
1. Az EEG készülék kalibrálása (5. ábra)
a. Az EEG bekapcsolása a hátsó panelen lévő ON/OFF gomb segítségével.
b. A papír elindítása a RECORD gomb lenyomásával történik.
c. Az általunk kívánt érzékenységi fokozat kiválasztásával és a CAL gomb lenyomásával mind a négy csatornán megjelenik a kalibráló jel.
d. A finombeállító segítségével a jeleket egyenlő szintre hozzuk.
e. A MÉRŐ gomb lenyomásával megjelenik az agykérgi alaptevékenység.
5. ábra 8 csatornás EEG készülék kapcsolópanel rajza
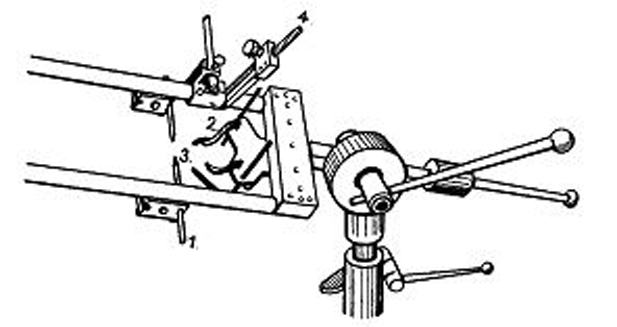
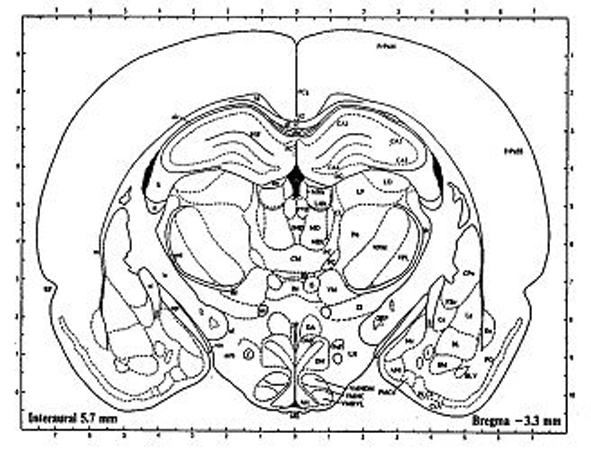
Az állatok ilyen kísérleti célra való előkészítésének részletes leírása a vonatkozó szakcikkek módszertani fejezetében megtalálható, e helyen csak az elvek nagyvonalú ismertetésére térünk ki. Előzetes, steril műtét alkalmával az altatott állat átfúrt koponyacsontján keresztül elvezető elektródokat ültetünk a kéreg felszínére, vagy süllyesztünk az agykéreg különböző mélységeibe. Ezután a koponyacsonton ejtett nyílásokat zárjuk, és az elektródokat fogászati cementtel a koponyacsonthoz rögzítjük és rövid vezetékek segítségével a fejtetőn az elvezető kábel csatlakoztatására alkalmas feltéthez kötjük. E műtét alkalmával gyakran az agykérgi idegsejtek későbbi ingerlésére céljából a különböző kéregalatti struktúrákba (pl. talamikus magvak, corpus callosum, stb.) ingerlő fémelektródot is beültethetünk. Erre a célra az állat koponyáját rögzítő, pontos beosztásokkal ellátott, mozgatható elektródtartó karokkal rendelkező stereotaxiás készülék (6. ábra), valamint az agy struktúráit a tér három síkjában pontos koordinátákkal feltérképező atlasz (7. ábra) szolgál. Az ilyen módon előkészített állatok a műtét után felépülve éber állapotban tanulási és alvási kísérletekben, epilepszia vizsgálatokban vagy más viselkedési megfigyelésekben szerepelhetnek.
Kísérlet közben az állatot az elektroenkefalográfhoz vagy a biológiai erősítőhöz a fejtetői konnektoron keresztül több eres kábel köti.
6. ábra Stereotaxiás készülék macskához. 1. Füldugasz; 2. Orbitarögzítő; 3. Állkapocsrögzítő; 4. elektródatartó
7. ábra Patkányagy koronális metszete
Valamely érzékszerv vagy afferens pálya impulzusszerű fiziológiás vagy elektromos ingerlésével keltett agykérgi elektromos jelenséget kiváltott potenciálnak (KP, EP) vagy eseményfüggő potenciálnak (event related potential, ERP) nevezzük. A tónusos jellegű EEG ritmusban a kiváltott potenciál többfázisú, egyszeri, időleges potenciál változást jelent. A kiváltott potenciálok gyakran az alap EEG potenciálokkal azonos nagyságrendbe tartozó kitérések, ezért a háttértevékenységből több, egymást követő kiváltott potenciál átlagolásával emelhetők ki. Ilyen potenciálok a zárt koponyatetőről is elvezethetők, és információt szolgáltatnak az afferens rendszer szerveződéséről és agykérgi képviseletéről. Valamely szenzoros pálya ingerlésével kiváltott potenciálok csak a megfelelő kérgi képviseletről vezethetők el. A kiváltott potenciálok klinikailag is hasznos eszközök az agy mindenkori aktivitásának, működőképességének objektív mérésére, valamint a különböző kérgi és kéregalatti folyamatok tanulmányozására.
Az amplitudó átlagolás módszere.
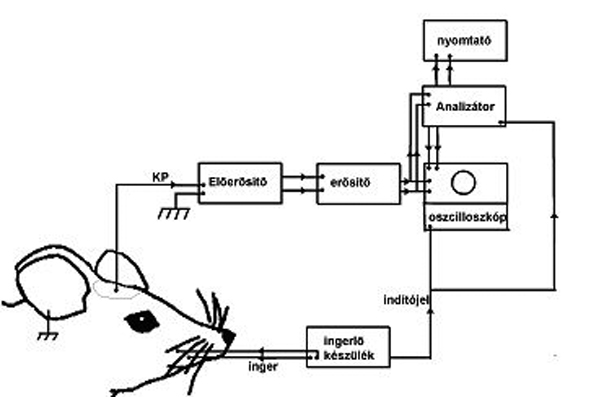
Az Average parancs egy számítógépes műveletet indít el. Ennek haszna a kiértékelés szempontjából az, hogy az egyedileg változékony kiváltott potenciálok jellegzetes, állandó elemeit megőrzi, véletlenszerű ingadozásaikat elhagyja. A művelet előfeltétele az, hogy (1) a sugárindítást az ingerlő végezze s azt az inger meghatározott idővel kövesse. (2) Az inger betörést az erősítő regisztrálja és az oszcilloszkóp sugarán megjeleníti. (3) Ezt követi a kiváltott potenciál megjelenése bizonyos latencia idő múltán (8. ábra).
A sugárindítást követő sugárlefutást az analóg-digitál (AD) konverter 1024 időszeletre osztja, és minden időszelet alatt beérkező feszültségértéket külön memória rekeszben rögzít. Ily módon a sugárlefutás a késleltetéssel, artefaktummal, latenciaidővel és a kiváltott potenciál konfigurációjával együtt egy 1024 rekeszre tagolódó fájlban raktározódik. A következő sugárlefutás eseményei a fix kiindulóponttól kezdődően meghatározott időpontokban érik el az egyes memória rekeszeket s azok tartalmához hozzáadódnak. Ugyanakkor az összeg a sugárátfutás sorszámának megfelelő számmal elosztódik. Így minden memória rekesz az addig érkezett feszültségértékek átlagát tartalmazza. Az átlagolni kívánt potenciálok számát előre meghatározzuk (pl. 20) és az adatgyűjtés 20 impulzus után leáll. Ekkor előhívva az 1024 memória rekesz tartalmát megkapjuk a regisztrált 20 potenciál átlagát, ami kifejezi ezen biológiai jelek releváns tulajdonságait.
8. ábra Kiváltott potenciálok elvezetése, átlagolása és kinyomtatása
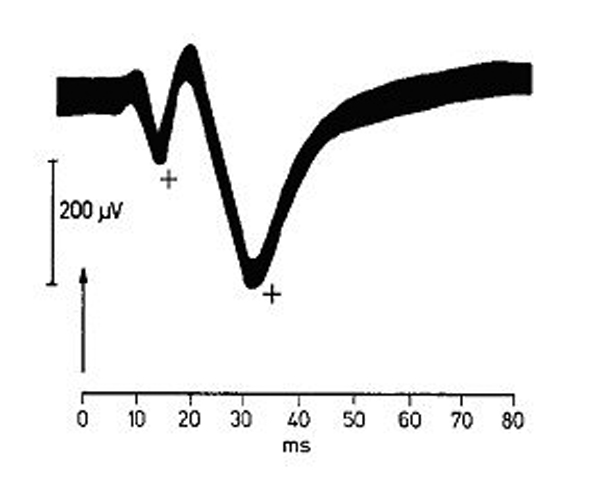
A n. ischiadicus elektromos ingerlésével a szomatoszenzoros kéreg felszínén kb. 5-12 ms-os latenciával egy korai kis amplitúdójú negatív-pozitív hullám váltható ki, amit egy 20-80 ms latenciájú nagyobb, elnyújtott pozitív kilengés követ (9. ábra). Az első hullám-szekvencia a primer kiváltott potenciál, a második a diffúz szekunder válasz, amit időnként egy nagy negatív hullám, vagy hullám sorozat követ. A primer válasz csak ott jelenik meg, ahol az adott érzékszervből eredő pályák végződnek. A szekunder válasz kevésbé lokalizált, egyidejűleg az elsődleges szenzoros área körüli területekről is elvezethető, feltehetőlen szubkortikális eredetű felszálló pályák aktivitásából ered.
9. ábra A n. ischiadicus ingerlésével (nyíl) kiváltott potenciál az ellenoldani érző kéregben barbituráttal altatott macskában. A felület-negativitást felfelé irányuló kitérés jelzi.
Szomatoszenzoros ingerlést leggyakrabban a n. ischiadicus, a n. radiális, vagy a n. trigeminus beidegzési területén alkalmazunk.
A patkány - éjszakai állat révén - legfontosabb szenzoros érzékszerve a bajusz rostok rendszere, mely a következő főbb struktúrákból áll:
•-szinuszszőrök (vibrisszák), a bajuszpárnán
•-n. trigeminus infraorbitális ága, melynek sejtjei a Gasser dúcban helyezkednek el,
•-a gerincvelői trigeminális magvak (nucl. principalis, sn. interpolaris, sn. oralis és sn. caudalis),
•-a talamusz ventro-posztero-medialis magja (VPM),
•-az elsődleges szomatoszenzoros kéreg postero-medialis területe (barrel kéreg).
A barrel kéreg nevét onnan kapta, hogy negyedik rétegében gyűrű alakú sejtcsoportosulások (barrelek) találhatók, melyek 1-1 perifériás szinuszszőr képviseletét jelentik. A szinuszszőrök ingerlése 7-9 ms latenciájú kiváltott potenciálokat kelt a barrel kéregben. Az elsődleges motoros kéreg vibrissza régiója az ellenoldali bajuszszőrök izmai mozgatásának iniciálásában és koordinálásában játszik fontos szerepet. Szoros és kölcsönös kapcsolatban van a szomszédos szomatoszenzoros kéreggel (részben át is fedik egymást). A motoros kéreg az információt döntő módon a szomatoszenzoros kéregből kapja, asszociatív kapcsolatok révén, így itt a kiváltott potenciálok latenciája is hosszabb (12-25 ms).
Elektromos ingerlésre két-pólusú tűelektródot szúrunk a bőr alá, melyet négyszögingerlő kimenetéhez csatlakoztatva szubmaximális erősségű, és jeltartamú, tetszőleges frekvenciájú elektromos impulzusokat bocsájthatunk az ingerelt helyre.
Rövid hangimpulzusokkal ingerelve, potenciálok válthatók ki a hallókérgen is. Ezek a potenciálok elvezethetők a hallókéreg fölött, magáról a hajas fejbőrről is, de állatkísérletben általában a feltárt hallókéreg felszínéről vezetjük el a hang ingerekkel kiváltott aktivitást. Kísérletekben gyakran alkalmaznak koppanásszerű hangot (un. click-et), mely különböző ferkvenciájú hangok keveréke. Hanggenerátorral előállíthatunk tiszta hangokat is.
Kísérletünkben a Medicor cég phonostimulátorával előállított különböző frekvenciájú tiszta hangokkal ingereljük az állat egyik vagy mindkét fülét (mon- ill. binaurális ingerlés).
Készülék beállítása: bekapcsolás után, nyomjuk be a Phone és a Gated gombokat. Állítsunk be 125 Hz frekvenciájú, 50 ms jeltartamú jeleket.
Az akusztikus kiváltott potenciálok elvezetése a fentebb már ismertetett módon történik. 1. Keressük meg ezen hangokkal kiváltott akusztikus kérgi válaszok punctum maximumát. 2. Itt vegyünk fel és átlagoljunk 50 jelet. 3. Mérjük meg az átlagolt kiváltott válasz pozitív és negatív csúcslatenciáit, amplitúdóját. 4. Rajzoljuk be a hallókéreg térképére a punctum maximum helyét. Ezen ingerléseket, elvezetéseket és a kiváltott válasz paramétereinek meghatározását végezzük el 250Hz, 500Hz, 1000 Hz, 2000 Hz, 4000 Hz és 8000 Hz frekvenciájú hang ingerek esetében is. 5. Ezután válasszuk ki az 1000 Hz frekvenciájú, 50 ms jeltartamú rövid sípoló hangot, és ezeket a jeleket adjuk 0.5, 1, 2, 5, 10, 20 és 50 cps gyakorisággal. Átlagoljuk az egyes gyakorisággal regisztrált kiváltott potenciálokat, mérjük meg amplitúdójukat (µV), majd a gyakoriság (cps) függvényében ábrázoljuk az amplitúdókat.
A szembe villantott fényingerrel a látókérgen válthatunk ki potenciálokat a koponya occipitalis régióján vagy a feltárt látókéregen. Más kísérletekben valamilyen sebességgel mozgó fényponttal, szakasszal ingerlik a szemet, vagy bonyolult ábrákat vetítenek a vizsgált egyén, vagy kísérleti állat elé. Egyszerűbb esetben azonban, még diagnosztikus célból is elégséges a látórendszer vizsgálatához, ha egy fényfelvillanás éri a szemet, a látókérgi kiváltott potenciál latenciájából, alaki viszonyaiból fiziológiai és orvosi szempontból is fontos következtetések vonhatók le.
Jelen kísérletünkben a Medicor cég Photostimulátorával, a készülék stroboszkópja segítségével adjuk a különböző paraméterű fényfelvillanásokat.
A készülék beállítása: a készülék bekapcsolása után nyomjuk be a Photo, Det, Delay, Discr kapcsolókat. 1 Hz frekvenciával adjuk a fényfelvillanásokat, melynek erősségét az Intensity gombokkal (I-V) állitsuk be úgy, hogy jól regisztrálható potenciálokat tudjunk a látókéregről elvezetni. 1. Keressük meg a kiváltott válaszok punctum maximumát. 2. Átlagoljunk 50 potenciált, mérjük meg a kiváltott potenciálok csúcslatenciáit, amlitúdóit. 3. Határozzuk meg az 0.5Hz, 1Hz, 2Hz, 5Hz, 10Hz és 20Hz frekvenciájú ingerléssel kiváltott és átlagolt jelek amplitúdóit, majd az amplitúdó értékeket ábrázoljuk a frekvencia függvényében.
A kiváltott potenciálok átlagolása az elvezetéssel párhuzamosan (on-line) vagy az eltárolt jelek visszajátszásával utólag (off-line) is történhet. A kapott görbék leggyakrabban mért értékei: a különböző csúcsok latencia ideje, a csúcsoknak az izoelektromos vonaltól mért amplitúdói, a pozitív-negatív komponensek csúcstól csúcsig mért amplitúdója, vagy a fél amplitúdónál mért hullámszélesség.
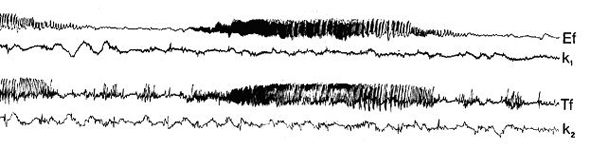
Kísérletes epilepszia fókusz kialakítására számos kémiai, mechanikai vagy elektromos módszer ismeretes. Az állatot a fentiekben ismertetett módon műtétileg előkészítjük. A gyors, korai K+- csatorna-blokkolóként ismert 3-aminopyridin kristályka az agykéreg felszínére helyezve 4-5 percen belül a humán temporális lebeny epilepsziához hasonló, fokális elektromos görcsrohamokat kelt. Az így kialakult elsődleges fókusz (Ef) kéregalatti és kommisszurális pályákon át az ellenoldali félteke megfelelő pontjaira is ráterjed. Ez a tükör fókusz (Tf, 10. ábra). E kísérleti paradigmával a humán epilepszia egyik legveszedelmesebb vonása, az epilepsziás állapot generalizációja vizsgálható. Kitűnő lehetőséget ad az apparátus az agykéreg farmakológiai befolyásolásának ellenőrzésére is. E modell alkalmas az epilepsziás működési zavar tanulmányozására, de egyéb farmakológiai és teszt vizsgálatokra is.
10. ábra Altatott patkány szomatomotoros agykérgén, 3-aminopyridinnel keltett epilepsziás görcsfókuszok roham-tevékenységének elektrokortikográfiás képe. Ef: elsődleges fókusz, Tf: tükör fókusz, k1 és k2: az Ef illetve Tf mögött 8 mm távolságra lévő agyi területek egyidejű EEG tevékenysége.
A kísérlet során a Nembutállal (Na-pentobarbitál, 45 mg/kg/ip) altatott, műtétileg előkészített állat koponyacsontján a feltárt jobboldali szomatoszenzoros kéreg (leendő Ef) mellett még három mélyedést készítünk fogászati fúró segítségével, egyet a Ef-al ellentlétes oldali azonos területről (Tf), illetve egyet-egyet a Ef-től és Tf-től hátra kb. 8 mm-re. A kísérlet során figyelemmel kísérjük az anesztézia mélységét, biztosítjuk a megfelelő hőmérsékletet és a kéreg felszínét fiziológiás sóoldattal védjük a kiszáradástól.